AGÊNCIA NACIONAL DE VIGILÂNCIA SANITÁRIA
DIRETORIA COLEGIADA
INSTRUÇÃO NORMATIVA - IN Nº 91, DE 27 DE MAIO DE 2021
(Publicada no DOU de 6-7-2022)
ANEXO I (*)
TESTES DE ACEITAÇÃO E DE CONTROLE DE QUALIDADE PARA SERVIÇOS DE FLUOROSCOPIA E RADIOLOGIA INTERVENCIONISTA
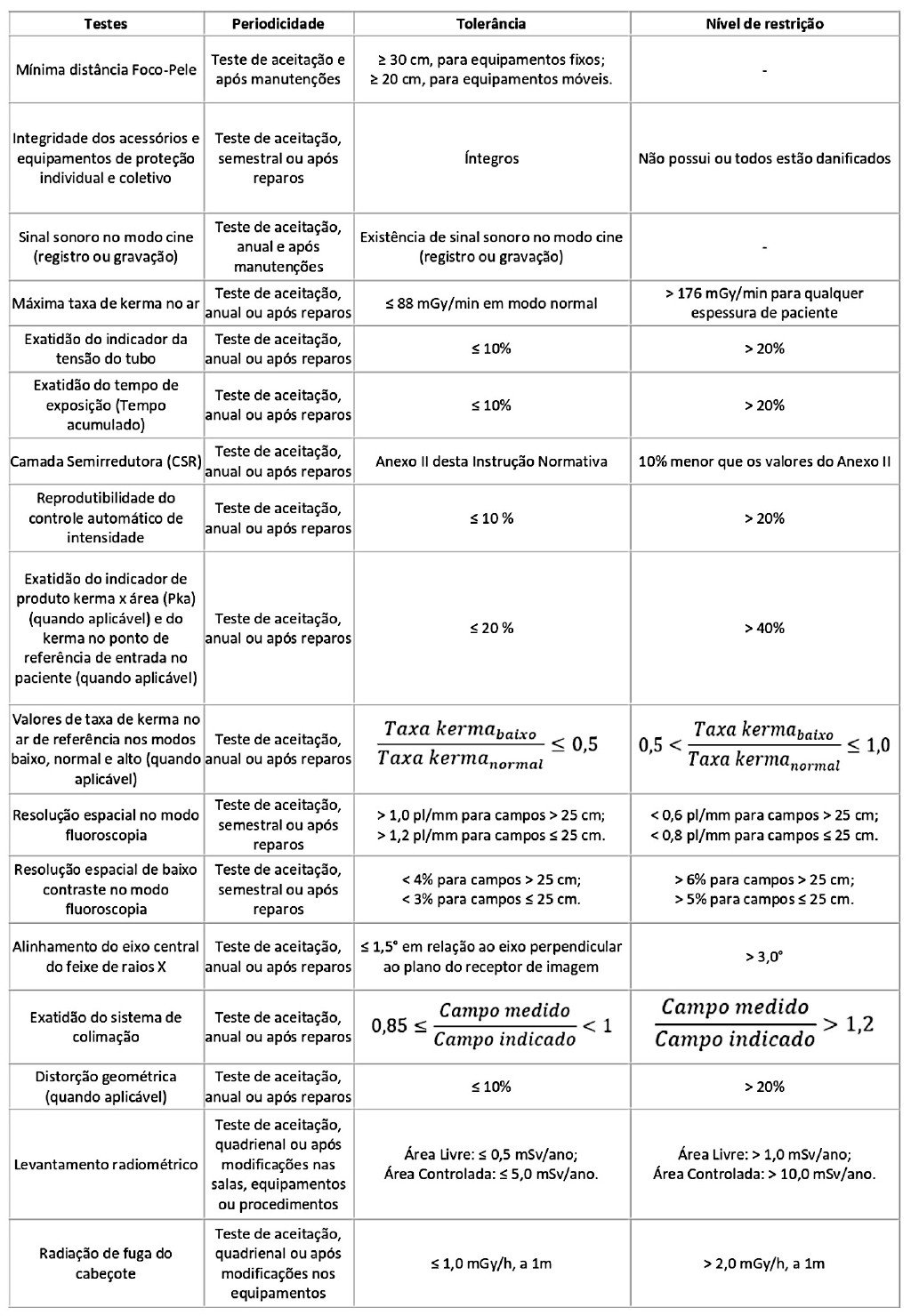
Publicada em parte por ter sido omitido no DOU de 6-7-2022, Seção 1, página 264.
RETIFICAÇÃO
Na Instrução normativa - IN n° 163, de 13 de julho de 2022, publicada no Diário Oficial da União n° 133, de 15 de julho de 2022, seção 1, pág. 127,
Onde se lê:
"Resolução de Diretoria Colegiada - RDC nº 732, de 7 de julho de 2022"
Leia-se:
"Resolução de Diretoria Colegiada - RDC nº 735, de 13 de julho de 2022"
Onde se lê:
"RDC nº 732/2022";
Leia-se:
"RDC nº 735/2022"
2ª DIRETORIA
COORDENAÇÃO DE PESQUISA CLÍNICA EM MEDICAMENTOS E PRODUTOS BIOLÓGICOS
RESOLUÇÃO-RE Nº 2.582, DE 9 DE AGOSTO DE 2022
O Coordenador de Pesquisa Clínica em Medicamentos e Produtos Biológicos, no uso das atribuições que lhe confere o art. 112, aliado ao art. 203, I, § 1º do Regimento Interno aprovado pela Resolução de Diretoria Colegiada - RDC nº 585, de 10 de dezembro de 2021, resolve:
Art. 1º Deferir petições relacionadas à Coordenação de Pesquisa Clínica em Medicamentos e Produtos Biológicos, conforme anexo.
Art. 2º Esta Resolução entra em vigor na data de sua publicação.
CLAUDIOSVAM MARTINS ALVES DE SOUSA
ANEXO
NOME DA EMPRESA CNPJ
MEDICAMENTO EXPERIMENTAL
CE
NÚMERO DE PROCESSO EXPEDIENTE
ASSUNTO DE PETIÇÃO
-------------------------------------------------------------------------------------------------------------------
ORPHANDC G IMPORTACAO E DISTRIBUICAO DE PRODUTOS FARMACEUTICOS LTDA - 22.566.515/0001-96
AT-752
66/2022
25351.881149/2021-68 4712744/21-9
10751 - ENSAIOS CLÍNICOS - Anuência em processo do Dossiê de Desenvolvimento Clínico de Medicamento (DDCM) de ORPCs - Sintético
25351.130276/2021-03 6257530/21-9
10483 - ENSAIOS CLÍNICOS - Anuência em Processo de Pesquisa Clínica de ORPC's - Medicamentos Sintéticos
Biozeus Biopharmaceutical S.A. - 16.828.860/0001-58
BZ371A
67/2022
25351.110298/2022-20 0715308/22-2
10750 - ENSAIOS CLÍNICOS - Anuência em processo do Dossiê de Desenvolvimento Clínico de Medicamento (DDCM) - Sintético
25351.119988/2022-44 0778756/22-1
10482 - ENSAIOS CLÍNICOS - Anuência em Processo de Pesquisa Clínica - Medicamentos Sintéticos
PHARMACEUTICAL RESEARCH ASSOCIATES LTDA - 03.762.871/0001-30
Acoramidis HCl
73/2019
25351.255609/2022-89 1449985/22-1
10818 - ENSAIOS CLÍNICOS - Modificação de DDCM - Inclusão de protocolo de ensaio clínico não previsto no plano inicial de desenvolvimento
PRODUTOS ROCHE QUÍMICOS E FARMACÊUTICOS S.A. - 33.009.945/0001-23
GDC-1971
68/2022
25351.049663/2022-97 0393034/22-3
10750 - ENSAIOS CLÍNICOS - Anuência em processo do Dossiê de Desenvolvimento Clínico de Medicamento (DDCM) - Sintético
25351.192057/2022-91 1156519/22-5
10818 - ENSAIOS CLÍNICOS - Modificação de DDCM - Inclusão de protocolo de ensaio clínico não previsto no plano inicial de desenvolvimento
RO7247669
25351.166461/2021-28 4199293/22-8
10820 - ENSAIOS CLÍNICOS - Modificação de DDCM - Alteração que potencialmente gera impacto na qualidade ou segurança do produto sob investigação
PRODUTOS ROCHE QUÍMICOS E FARMACÊUTICOS S.A. - 33.009.945/0001-23
RO7247669
71/2022
25351.166461/2021-28 0937460/21-4
10754 - ENSAIOS CLÍNICOS - Anuência em processo do Dossiê de Desenvolvimento Clínico de Medicamento (DDCM) - Produtos Biológicos
25351.182191/2022-83 4408681/22-4
10818 - ENSAIOS CLÍNICOS - Modificação de DDCM - Inclusão de protocolo de ensaio clínico não previsto no plano inicial de desenvolvimento
25351.166461/2021-28 4199293/22-8
10820 - ENSAIOS CLÍNICOS - Modificação de DDCM - Alteração que potencialmente gera impacto na qualidade ou segurança do produto sob investigação
25351.202925/2022-58 4432213/22-5
Pralsetinibe
34/2022
10818 - ENSAIOS CLÍNICOS - Modificação de DDCM - Inclusão de protocolo de ensaio clínico não previsto no plano inicial de desenvolvimento
AZIDUS BRASIL PESQUISA CIENTIFICA E DESENVOLVIMENTO LTDA - 07.743.272/0001-20
Firibastat
50/2020
25351.530884/2022-97 2684701/22-9
10818 - ENSAIOS CLÍNICOS - Modificação de DDCM - Inclusão de protocolo de ensaio clínico não previsto no plano inicial de desenvolvimento
BRISTOL-MYERS SQUIBB FARMACÊUTICA LTDA - 56.998.982/0001-07
Nivolumabe
36/2016
25351.336600/2017-19 0698466/22-5
10824 - ENSAIOS CLÍNICOS - Emenda Substancial a Protocolo Clínico
GLAXOSMITHKLINE BRASIL LTDA - 33.247.743/0001-10
RSVPreF3
79/2021
25351.477506/2020-14 3333174/21-0
10824 - ENSAIOS CLÍNICOS - Emenda Substancial a Protocolo Clínico
25351.477506/2020-14 2464786/22-1
10824 - ENSAIOS CLÍNICOS - Emenda Substancial a Protocolo Clínico
25351.334183/2021-48 2464788/22-8
10824 - ENSAIOS CLÍNICOS - Emenda Substancial a Protocolo Clínico
ABBVIE FARMACÊUTICA LTDA. - 15.800.545/0001-50
Venetoclax
1/2016
25351.626338/2015-01 4258913/22-4
10820 - ENSAIOS CLÍNICOS - Modificação de DDCM - Alteração que potencialmente gera impacto na qualidade ou segurança do produto sob investigação
ALEXION FARMACEUTICA BRASIL IMPORTACAO E DISTRIBUICAO DE PRODUTOS E SERVICOS DE ADMINISTRACAO - 10.284.284/0001-49
Ravulizumabe
40/2017
25351.458496/2016-08 4356526/22-3
10820 - ENSAIOS CLÍNICOS - Modificação de DDCM - Alteração que potencialmente gera impacto na qualidade ou segurança do produto sob investigação
WYETH INDÚSTRIA FARMACÊUTICA LTDA - 61.072.393/0001-33
Nirmatrelvir
72/2021
25351.787136/2021-01 4374130/22-4
10820 - ENSAIOS CLÍNICOS - Modificação de DDCM - Alteração que potencialmente gera impacto na qualidade ou segurança do produto sob investigação
PTC FARMACEUTICA DO BRASIL LTDA. - 25.210.463/0001-09
PTC923
42/2022
25351.459655/2021-74 4271692/22-6
10820 - ENSAIOS CLÍNICOS - Modificação de DDCM - Alteração que potencialmente gera impacto na qualidade ou segurança do produto sob investigação
ASTRAZENECA DO BRASIL LTDA - 60.318.797/0001-00
AZD1222
38/2020
25351.490586/2020-95 4280295/22-4
10824 - ENSAIOS CLÍNICOS - Emenda Substancial a Protocolo Clínico
AZD2936
69/2022
25351.197414/2022-15 2691615/22-1
10824 - ENSAIOS CLÍNICOS - Emenda Substancial a Protocolo Clínico
RESOLUÇÃO-RE Nº 2.583, DE 9 DE AGOSTO DE 2022
O Coordenador de Pesquisa Clínica em Medicamentos e Produtos Biológicos, no uso das atribuições que lhe confere o art. 112, aliado ao art. 203, I, § 1º do Regimento Interno aprovado pela Resolução de Diretoria Colegiada - RDC nº 585, de 10 de dezembro de 2021, resolve:
Art. 1º Autorizar a implementação das petições relacionadas à Coordenação de Pesquisa Clínica em Medicamentos e Produtos Biológicos, por decurso de prazo (art. 36, Resolução de Diretoria Colegiada - RDC nº 09/2015 e art. 36-A, Resolução de Diretoria Colegiada - RDC n° 573/2021), conforme anexo.
Art. 2º Esta Resolução entra em vigor na data de sua publicação.
CLAUDIOSVAM MARTINS ALVES DE SOUSA
ANEXO
NOME DA EMPRESA CNPJ
MEDICAMENTO EXPERIMENTAL
CE/DI
NÚMERO DE PROCESSO EXPEDIENTE
ASSUNTO DE PETIÇÃO
-------------------------------------------------------------------------------------------------------------------
i3 latin america brasil serviços de pesquisa clínica ltda - 08.190.722/0001-68
Sibeprenlimabe
61/2022
25351.101866/2022-00 0674669/22-1
10755 - ENSAIOS CLÍNICOS - Anuência em processo do Dossiê de Desenvolvimento Clínico de Medicamento (DDCM) de ORPCs - Produtos Biológicos
25351.125945/2022-06 0812415/22-9
10478 - ENSAIOS CLÍNICOS - Anuência em Processo de Pesquisa Clínica de ORPC's - Produtos Biológicos
ASTRAZENECA DO BRASIL LTDA - 60.318.797/0001-00
AZD2936
69/2022
25351.187932/2022-12 1138679/22-7
10754 - ENSAIOS CLÍNICOS - Anuência em processo do Dossiê de Desenvolvimento Clínico de Medicamento (DDCM) - Produtos Biológicos
25351.197414/2022-15 1183167/22-7
10479 - ENSAIOS CLÍNICOS - Anuência em Processo de Pesquisa Clínica - Produtos Biológicos
ELI LILLY DO BRASIL LTDA - 43.940.618/0001-44
LY3209590
70/2022
25351.187933/2022-67 1138682/22-7
10754 - ENSAIOS CLÍNICOS - Anuência em processo do Dossiê de Desenvolvimento Clínico de Medicamento (DDCM) - Produtos Biológicos
25351.274464/2022-15 1547283/22-3
10479 - ENSAIOS CLÍNICOS - Anuência em Processo de Pesquisa Clínica - Produtos Biológicos
Tirzepatida
18/2019
25351.533769/2022-74 2691772/22-6
10818 - ENSAIOS CLÍNICOS - Modificação de DDCM - Inclusão de protocolo de ensaio clínico não previsto no plano inicial de desenvolvimento
RESOLUÇÃO-RE Nº 2.584, DE 9 DE AGOSTO DE 2022
O Coordenador de Pesquisa Clínica em Medicamentos e Produtos Biológicos, no uso das atribuições que lhe confere o art. 112, aliado ao art. 203, I, § 1º do Regimento Interno aprovado pela Resolução de Diretoria Colegiada - RDC nº 585, de 10 de dezembro de 2021, resolve:
Art. 1º Publicar a desistência a pedido das petições/processos relacionadas à Coordenação de Pesquisa Clínica em Medicamentos e Produtos Biológicos, conforme anexo.
Art. 2º Esta Resolução entra em vigor na data de sua publicação.
CLAUDIOSVAM MARTINS ALVES DE SOUSA
ANEXO
|
Razão Social - CNPJ |
Nº de Processo |
Expediente da petição/Processo |
Expediente do Pedido de Desistência |
Assunto |
|
20.307.414/0001-75 |
25351.044796/2022-77 |
0347403/22-8 |
4378028/22-1 |
10751 - ENSAIOS CLÍNICOS - Anuência em processo do Dossiê de Desenvolvimento Clínico de Medicamento (DDCM) de ORPCs - Sintético |
|
20.307.414/0001-75 |
25351.049657/2022-30 |
0393014/22-9 |
4378198/22-3 |
10483 - ENSAIOS CLÍNICOS - Anuência em Processo de Pesquisa Clínica de ORPC's - Medicamentos Sintéticos |
|
61.072.393/0001-33 |
25351.601339/2021-10 |
4307694/22-7 |
4397394/22-9 |
10824 - ENSAIOS CLÍNICOS - Emenda Substancial a Protocolo Clínico |
|
61.821.344/0001-56 |
25351.296229/2019-07 |
4254406/22-8 |
4460539/22-5 |
10481 - ENSAIOS CLÍNICOS - Notificação de Término de Ensaio Clínico no Brasil |
RESOLUÇÃO-RE Nº 2.585, DE 9 DE AGOSTO DE 2022
O Coordenador de Pesquisa Clínica em Medicamentos e Produtos Biológicos, no uso das atribuições que lhe confere o art. 112, aliado ao art. 203, I, § 1º do Regimento Interno aprovado pela Resolução de Diretoria Colegiada - RDC nº 585, de 10 de dezembro de 2021, resolve:
Art. 1º Publicar o cancelamento a pedido das petições/processos relacionadas à Coordenação de Pesquisa Clínica em Medicamentos e Produtos Biológicos, conforme anexo.
Art. 2º Esta Resolução entra em vigor na data de sua publicação.
CLAUDIOSVAM MARTINS ALVES DE SOUSA
ANEXO
|
Razão Social - CNPJ |
Nº de Processo |
Expediente da petição/Processo |
Expediente do Pedido de Cancelamento |
Assunto |
|
04.611.797/0001-14 |
25351.023701/2021-09 |
8451571/21-6 |
4469158/22-4 |
10755 - ENSAIOS CLÍNICOS - Anuência em processo do Dossiê de Desenvolvimento Clínico de Medicamento (DDCM) de ORPCs - Produtos Biológicos |
|
08.190.722/0001-68 |
25351.035601/2021-17 |
8471221/21-0 |
4372041/22-5 |
10483 - ENSAIOS CLÍNICOS - Anuência em Processo de Pesquisa Clínica de ORPC's - Medicamentos Sintéticos |
|
00.251.699/0001-62 |
25351.126013/2022-72 |
4307669/22-6 |
4457394/22-0 |
10478 - ENSAIOS CLÍNICOS - Anuência em Processo de Pesquisa Clínica de ORPC's - Produtos Biológicos |
|
18.774.815/0001-93 |
25351.682571/2021-32 |
2500074/21-8 |
4461859/22-3 |
10479 - ENSAIOS CLÍNICOS - Anuência em Processo de Pesquisa Clínica - Produtos Biológicos |
GERÊNCIA-GERAL DE PRODUTOS BIOLÓGICOS, RADIOFÁRMACOS, SANGUE, TECIDOS, CÉLULAS, ÓRGÃOS E PROD DE TERAPIAS AVAN
RESOLUÇÃO-RE Nº 2.576, DE 8 DE AGOSTO DE 2022
A Gerente-Geral substituta de Produtos Biológicos, Radiofármacos, Sangue, Tecidos, Células, Órgãos e Produtos de Terapia Avançada da Agência Nacional de Vigilância Sanitária, no uso das atribuições que lhe foram conferidas pelo art. 112, aliado ao art. 203, I, § 1º do Regimento Interno aprovado pela Resolução de Diretoria Colegiada - RDC nº 585, de 10 de dezembro de 2021, resolve:
Art. 1º Conceder à empresa, constante no anexo, a renovação da Certificação de Boas Práticas de Fabricação (CBPF) de Produto de Terapia Avançada.
Parágrafo único. A presente certificação terá validade de 2 (dois) anos a partir de sua publicação.
Art. 2 o Esta Resolução entra em vigor na data de sua publicação.
PATRICIA KOTT TOMAZETT
ANEXO
Fabricante: Spark Therapeutics, Inc.
Endereço: 3737 Market St., Suite 1.300, Philadelphia, Pennsylvania PA 19104
País: Estados Unidos da América Código Único: H.000006
Solicitante: Novartis Biociências S.A. CNPJ: 56.994.502/0027-79
Autorização de Funcionamento: 1.00068-5 Expediente: 0346416/22-1
Renovação (Certificação de BPF) de Componente Ativo de Produto de Terapia Gênica de indústria internacional
3ª DIRETORIA
GERÊNCIA-GERAL DE TOXICOLOGIA
CONSULTA PÚBLICA Nº 1.107, DE 4 DE AGOSTO DE 2022
O Gerente-Geral de Toxicologia, no exercício da competência que lhe foi delegada por meio do Despacho 153, de 27 de outubro de 2021, aliado ao art. 187, III, do Regimento Interno aprovado pela Resolução de Diretoria Colegiada - RDC nº 585, de 10 de dezembro de 2021, resolve submeter à consulta pública, para comentários e sugestões do público em geral, proposta de ato normativo, em Anexo.
Art. 1º Fica aberto, a contar da data de publicação desta Consulta Pública, o prazo de 60 (sessenta) dias para que sejam apresentadas críticas e sugestões relativas à proposta de Instrução Normativa - IN que atualiza as Monografias dos Ingredientes Ativos de Agrotóxicos, Saneantes Desinfestantes e Preservativos de Madeira, publicada por meio da Instrução Normativa - IN n°103, de 19 de outubro de 2021.
Art. 2º A proposta supracitada estará disponível na íntegra no endereço eletrônico: http://antigo.anvisa.gov.br/consultas-publicas# e as sugestões deverão ser encaminhadas por escrito, em formulário próprio, para o endereço: Agência Nacional de Vigilância Sanitária, Gerência Geral de Toxicologia, SIA Trecho 5, Área Especial 57, Brasília/DF, CEP 71.205-050, ou para o e-mail: Este endereço de e-mail está protegido contra spambots. Você deve habilitar o JavaScript para visualizá-lo. .
§1° O formulário para envio de contribuições permanecerá à disposição dos interessados no endereço eletrônico https://www.gov.br/anvisa/pt-br/centraisdeconteudo/publicacoes/agrotoxicos/formulario-padrao-consulta-publica-ggtox.docx/view.
§2° As contribuições recebidas serão públicas e permanecerão à disposição de todos no site da Anvisa.
§3° As contribuições não enviadas no formulário de que trata o parágrafo anterior ou recebidas fora do prazo não serão consideradas para efeitos de consolidação do texto final do regulamento.
Art. 3º Findo o prazo estipulado no art. 1º, a Agência Nacional de Vigilância Sanitária promoverá a análise das contribuições e, após a deliberação da Diretoria Colegiada, disponibilizará o resultado da consulta pública no site da Anvisa.
Parágrafo único. A Agência poderá, conforme necessidade e razões de conveniência e oportunidade, articular-se com os órgãos e entidades envolvidos e aqueles que tenham manifestado interesse na matéria para subsidiar posteriores discussões técnicas e deliberação final da Diretoria Colegiada.
CARLOS ALEXANDRE OLIVEIRA GOMES
GERENTE-GERAL DE TOXICOLOGIA
ANEXO
PROPOSTA EM CONSULTA PÚBLICA
Processos nº: 25351.724646/2012-85, 25351.220797/2016-58, 25351.095628/2018-63, 25000.010898/93-55, 25351.015817/2021-05, 25351.067471/2019-04, 25351.728357/2008-01, 25351.171350/2021-33, 25351.220797/2016-58, 25000.009231/90-67, 25351.014315/2021-01, 25351.171350/2021-33, 25000.007285/96-19, 25351.095628/2018-63, 25001.024877/84 e 25351.067471/2019-04
Assunto: Proposta de Alteração das Monografia de ingredientes na Relação de Ingredientes Ativos de Agrotóxicos, Saneantes Desinfestantes e Preservativos de Madeira, publicada por meio da Instrução Normativa - IN N° 103, de 19 de outubro de 2021.
Área responsável: Gerência-Geral de Toxicologia - GGTOX
Relatora: Meiruze Sousa Freitas
4ª DIRETORIA
GERÊNCIA-GERAL DE INSPEÇÃO E FISCALIZAÇÃO SANITÁRIA
RESOLUÇÃO-RE Nº 2.587, DE 9 DE AGOSTO DE 2022
A Gerente-Geral de Inspeção e Fiscalização Sanitária, no uso das atribuições que lhe confere o art. 140, aliado ao art. 203, I, § 1º do Regimento Interno aprovado pela Resolução de Diretoria Colegiada - RDC nº 585, de 10 de dezembro de 2021, e o art. 6º, da Lei nº 9.782, de 26 de janeiro de 1999, resolve:
Art. 1º Adotar a medida preventiva constante no ANEXO.
Art. 2º Esta Resolução entra em vigor na data de sua publicação.
ANA CAROLINA MOREIRA MARINO ARAUJO
ANEXO
Empresa: INVERTMAX - MANIPULACAO E COMERCIO DE DEFENSIVOS NATURAIS LTDA - CNPJ: 10648925000105
Produto - (Lote): INVERTEMAX BIOINSETICIDA NATURAL(TODOS);
Tipo de Produto: Saneantes
Expediente nº: 4525720/22-5
Assunto: 70351 - Ações de Fiscalização em Vigilância Sanitária
Ações de fiscalização: Apreensão, Proibição - Comercialização, Distribuição, Fabricação, Propaganda, Uso
Motivação: Considerando a comercialização, exposição à venda e fabricação do produto sem registro por empresa sem autorização de funcionamento para a fabricação infringindo os arts. 2º e 12 da Lei 6360, de 23 de setembro de 1976 e tendo em vista o previsto nos art 6º e inciso I do art. 67 da Lei 6360, de 23 de setembro de 1976 e inciso XV do art. 7º da Lei 9782, de 26 de janeiro de 1999.
(DOU de 10.08.2022 – págs. 295 a 297 – Seção 1)


