Disponíveis materiais preparatórios para o diálogo setorial sobre revisão da rotulagem geral de alimentos
Encontro será realizado no dia 4 de setembro, às 9h30.
Em cumprimento ao seu compromisso de transparência e fortalecimento da participação social, a Anvisa disponibilizou os documentos preparatórios para o diálogo setorial virtual sobre a revisão do regulamento de rotulagem geral de alimentos. O encontro será realizado na próxima quinta-feira (4/9), das 9h30 às 12h, pelo Microsoft Teams.
Veja abaixo os documentos:
1) Planilha com a proposta comentada de consulta pública, contendo:
- comparação dos dispositivos da RDC 727/2022 com os do Projeto de Resolução Mercosul sobre rotulagem geral;
- proposta de revisão da RDC 727/2022; e
- esclarecimentos adicionais relativos às alterações propostas.
2) Minuta da consulta pública, contendo a redação completa da proposta normativa que será submetida à deliberação da Diretoria Colegiada.
Esses documentos visam subsidiar o debate com base em análise técnico-normativa, especialmente útil para agentes do setor regulado, sociedade civil e demais interessados.
Objetivo do encontro
O diálogo setorial terá como foco a apresentação das principais alterações acordadas no âmbito do Mercosul para a rotulagem geral de alimentos embalados, além de esclarecer eventuais dúvidas que possam qualificar a participação na fase de consulta pública.
Como participar
O evento é aberto a todos os setores da sociedade e não requer inscrição prévia.
Para participar, acesse o link Diálogo setorial virtual sobre revisão do regulamento de rotulagem geral de alimentos.
CMED divulga Anuário Estatístico do Mercado Farmacêutico
Documento apresenta os dados de 2024 e ajuda a compreender o desempenho e a dinâmica do setor farmacêutico nacional.
A Secretaria Executiva da Câmara de Regulação do Mercado de Medicamentos (SCMED) divulgou a 8ª edição do Anuário Estatístico do Mercado Farmacêutico.
A publicação reafirma o compromisso da Câmara de Regulação do Mercado de Medicamentos (CMED) com a transparência e consolida as informações oficiais do Sistema de Acompanhamento do Mercado de Medicamentos (Sammed), oferecendo uma visão abrangente do setor em 2024. O documento não interpreta causas ou políticas, mas disponibiliza uma base sólida para análises independentes de pesquisadores, gestores e reguladores.
Assim como na edição anterior, o Anuário 2024 conta com o Anexo Estatístico, em formato .XLS, que detalha os principais indicadores do mercado. O material foi desenvolvido para facilitar a análise aprofundada das informações, ampliando a capacidade de compreensão sobre o desempenho e a dinâmica do setor.
O levantamento considerou dados consolidados do ano de 2024, extraídos dos relatórios de comercialização encaminhados pelas empresas. Além das substâncias e classes terapêuticas mais comercializadas, contém estatísticas sobre faturamento, quantidade de unidades vendidas, características dos medicamentos, porte das empresas e canais de distribuição.
Dados gerais
De acordo com o Anuário, o mercado farmacêutico brasileiro alcançou um faturamento de aproximadamente R$ 160,7 bilhões em 2024, representando um crescimento nominal de 12,9% em relação a 2023. Foram comercializadas 6,07 bilhões de embalagens, um aumento de 5,2% em relação ao ano anterior, abrangendo um total de 14.586 tipos de apresentações.
O setor contou com a participação de 232 empresas, responsáveis por 7.289 nomes comerciais de produtos, distribuídos em 514 classes terapêuticas diferentes. Além disso, foram comercializados 1.944 diferentes princípios ativos, refletindo a diversidade e a complexidade do mercado brasileiro.
Confira abaixo um resumo do panorama geral do mercado farmacêutico em 2024.
Anvisa fortalece cooperação regulatória com a Cofepris
Agências do Brasil e do México assinaram um Memorando de Entendimento.

Nos dias 27 e 28 de agosto (quarta e quinta-feira), a Anvisa integrou a missão oficial do vice-presidente do Brasil, Geraldo Alckmin, ao México. O diretor-presidente substituto da Agência, Rômison Rodrigues Mota, participou da mesa setorial de saúde organizada pela ApexBrasil e acompanhou reuniões da agenda oficial, incluindo encontro com o secretário de Saúde do México, David Kershenobich Stalnikowitz, e com a comissionada da autoridade reguladora mexicana Cofepris (Comissão Federal para Proteção contra Riscos Sanitários), Armida Zúniga Estrada.
Um dos resultados da missão foi a assinatura de um novo Memorando de Entendimento entre a Anvisa e a Cofepris, que amplia a cooperação em temas estratégicos como confiança regulatória (reliance) e troca de informações.
Nos últimos anos, as duas autoridades reguladoras têm avançado em iniciativas de confiança regulatória. Como resultado dessas iniciativas, a Cofepris reconheceu a Anvisa como Autoridade Reguladora de Referência para: registro sanitário expedito de dispositivos médicos; e reconhecimento dos Certificados de Boas Práticas de Fabricação (CBPF) de fármacos, medicamentos e dispositivos médicos emitidos pela Anvisa.
Por sua vez, a Anvisa reconheceu a Cofepris como Autoridade Reguladora Estrangeira Equivalente para a Certificação de Boas Práticas de Fabricação (CBPF) de medicamentos.
Essas medidas reduzem custos, facilitam o comércio bilateral e ampliam o acesso da população a tecnologias modernas e inovadoras.
A assinatura do novo Memorando de Entendimento reforça ainda a cooperação e é mais um passo importante da Anvisa para fortalecer a integração regional e a confiança regulatória internacional.
Confira a íntegra do Memorando de Entendimento aqui.
Anvisa e MGI reafirmam compromisso com a transformação digital
Órgãos assinaram parceria para o quarto ciclo do Plano de Transformação Digital da Agência.

MGI promove encontro de órgãos federais que assinaram Planos de Transformação Digital.
A Anvisa e a Secretaria de Governo Digital (SGD) do Ministério da Gestão e Inovação em Serviços Públicos (MGI) assinaram, na tarde da última terça-feira (26/8), o quarto ciclo do Plano de Transformação Digital (PTD) da Agência, referente ao biênio 2025-2026. O gerente-geral de Tecnologia da Informação, Jorge Carvalho, representou a Anvisa no evento.
O objetivo do plano é oferecer serviços públicos de melhor qualidade, mais simples, acessíveis, a qualquer hora e lugar, e a um custo menor para o cidadão.
A Anvisa é o órgão brasileiro com o maior número de serviços transformados digitalmente (382) disponíveis no Portal Gov.br, conforme o quadro abaixo:
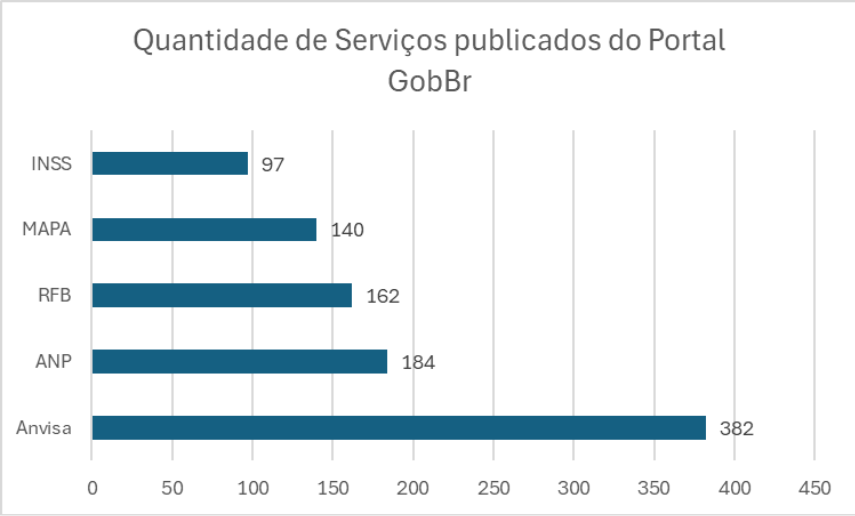
Quantidade de serviços publicados no gov.brFonte: Painel de monitoramento de serviços federais — Governo Digital
A implantação do Solicita (plataforma eletrônica de submissão de peticionamentos à Anvisa) é responsável pela transformação de 84% dos serviços e está integrada ao PagTesouro, ao API de avaliação do usuário (ferramenta para avaliar a qualidade de serviços) e ao login único.
Uma das parcerias entre a Agência e a SGD é o projeto especial e-Notivisa — um sistema lançado em março de 2023, que permite a notificação, pelo cidadão, de queixas técnicas e eventos adversos. O projeto foi desenvolvido por meio de iniciativa Startup Gov.br, e, atualmente, continua em evolução com uma equipe específica da Anvisa, pelo modelo ágil.
Os órgãos também são parceiros no Projeto Titan (Transformação da Infraestrutura de Tecnologia da Anvisa), que será concluído em novembro deste ano.
PTD 2025-2026
O Plano de Transformação Digital da Anvisa para 2025/2026 é organizado em cinco eixos, que seguem a estrutura e as diretrizes da Estratégia de Governo Digital (EGD), instituída por meio do Decreto 10.332/2020. A EGD está organizada em princípios, objetivos e iniciativas que norteiam a transformação do governo, por meio de tecnologias digitais. Os eixos se referem aos seguintes aspectos:
- Eixo 1 – Serviços Digitais e Melhoria da Qualidade.
- Eixo 2 – Unificação de Canais Digitais.
- Eixo 3 – Gestão e Governança de Dados.
- Eixo 4 – Segurança e Privacidade.
- Projetos especiais.
Neste ciclo, estão previstas 106 ações detalhadas no Anexo de Entregas do PTD 2025-2026, sendo que 84 dessas ações integram o eixo de serviços digitais prestados no sistema Solicita, incluindo:
- Melhorias nos formulários de Autorização de Funcionamento de Empresa (AFE).
- Inclusão de formulários específicos no Solicita para áreas como GGMED, Copec, GGBIO, GGCOS, GGTAB, GGFIS, Coafe, GGTOX, GGPAF e GGTPS. Com isso, busca-se a substituição completa do peticionamento antigo pelo Solicita (Diretriz Asp Zero).
- Solução para a emissão de certidões e certificados com fluxos padronizados para as áreas negociais – que tem como objetivo ampliar a modalidade de autosserviço para a emissão eletrônica de certidões e certificados, até agora contemplando produtos cosméticos, saneantes registrados e notificados e autorização de funcionamento (também serão incluídos dispositivos médicos, alimentos e medicamentos).
Outras 22 ações integram os demais eixos de transformação digital, abrangendo:
- Soluções para inativação do portal antigo (Alertas e Fale Conosco).
- Integração do Portal com o Siscomex e a Duimp (fluxo das Licenças de Importação – LIs).
- Implementação de API para o Portal de Consultas Externas.
- Conclusão dos quatro projetos apoiados pelo programa Startup Finep.
- Ações obrigatórias para atendimento ao Framework de Privacidade e Segurança da Informação (ciclos PPSI/SGD).
Destaque
Os serviços da Anvisa estão bem avaliados na nota média no ranking das 5 estrelas (1ª posição):
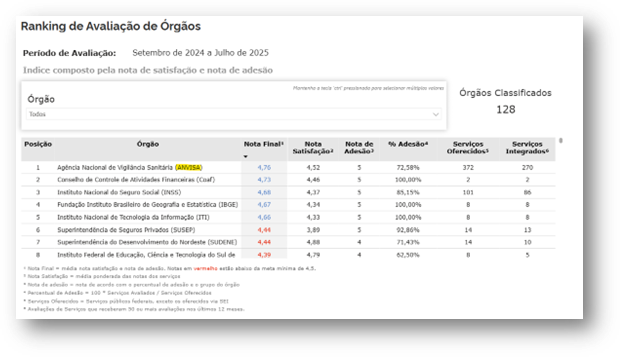
Fonte: Ranking de serviços e de órgãos — Governo Digital
Anvisa esclarece dúvidas sobre serviços que realizam exames de análises clínicas
O documento de Perguntas & Respostas aborda questões sobre a RDC 978/2025.
A Anvisa divulgou, nesta quarta-feira (27/8), um documento com perguntas e respostas sobre as novas regras para os serviços que fazem exames de análises clínicas (EACs), como exames de sangue, urina etc.
A 1ª edição do documento de Perguntas & Respostas esclarece as principais dúvidas sobre a RDC 978/2025, que entrou em vigor no dia 10 de junho. O objetivo é facilitar a aplicação correta das novas regras, tanto pelos órgãos de vigilância sanitária quanto pelo setor regulado (como laboratórios, clínicas, farmácias e consultórios).
O documento deve ser atualizado sempre que surgirem novas dúvidas ou quando as regras forem ajustadas. Esta primeira versão inclusive já contém as mudanças feitas pela RDC 986, publicada em 15 de agosto de 2025.
É importante lembrar que o material tem caráter orientativo, ou seja, serve como guia, e faz parte de um conjunto de ações educativas promovidas pela Anvisa.
Sobre a nova resolução (RDC 978/2025)
A nova norma foi aprovada pela Diretoria Colegiada da Anvisa em 4 de junho deste ano, durante a 8ª Reunião Ordinária Pública. Ela substitui a resolução anterior (RDC 786/2023) e traz atualizações importantes sobre o funcionamento dos serviços de exames laboratoriais.
A elaboração do documento de Perguntas & Respostas contou com a participação de representantes do setor público e privado. A ideia foi reunir as dúvidas mais frequentes e apresentar respostas que ajudem na correta interpretação e aplicação da nova regra.
Fonte: Anvisa, em 28.08.2025.


