Webinar orienta setor regulado sobre estudos de degradação em medicamentos
Encontro será no dia 14 de abril, às 10h. Participe!
A Anvisa irá realizar um webinar para orientar o setor regulado quanto aos novos requisitos para condução dos estudos de degradação forçada e controle de produtos de degradação em medicamentos.
A norma traz uma abordagem mais científica, com a possibilidade de redução de testes e qualificação mais racional de produtos de degradação, além de estratégias que podem diminuir o uso de modelos animais.
O encontro será na próxima segunda-feira, dia 14 de abril, às 10h. Para participar, basta clicar no link abaixo, no dia e horário agendados.
14/4, às 10h – Webinar - Entendendo a RDC 964/2025 - Estudos de Degradação Forçada em Medicamentos e Insumos
Webinar
É um seminário virtual que tem como objetivo fortalecer as iniciativas de transparência da Anvisa, levando conteúdo e conhecimento atualizados ao público. A transmissão é via web e a interação com os usuários é feita em tempo real, por um chat realizado durante o evento.
Confira a página específica de webinares realizados pela Agência.
Webinar aborda implementação do WhoDrug para notificação de eventos adversos de medicamentos
Encontro será no dia 14 de abril, às 15h. Participe!
A Anvisa irá realizar, na próxima segunda-feira (14/4), um webinar com o tema “Implementação do WhoDrug – Alteração da RDC 406/2020”.
Durante o encontro, a Agência irá esclarecer dúvidas sobre a publicação da RDC 967, de 18 de março de 2025, que alterou a RDC 406, de 22 de julho de 2020. A nova norma torna obrigatório o uso do WHODrug (C3) na codificação da notificação de suspeita de eventos adversos pelas empresas no VigiMed. As empresas de medicamentos têm o prazo de 1 ano para adequação.
O WHODrug é um dicionário de medicamentos e vacinas de referência internacional, que dá suporte à implementação dos padrões ISO IDMP de identificação de medicamentos – requisito previsto nos Guias do ICH (International Council for Harmonisation of Technical Requirements for Pharmaceuticals for Human Use – Conselho Internacional sobre Harmonização de Requisitos Técnicos em Produtos Farmacêuticos para Uso Humano).
Para participar do evento, basta clicar no link abaixo, no dia e horário agendados.
14/4, às 15h – Webinar: Implementação do WhoDrug - Alteração da RDC 406/2020
Webinar
É um seminário virtual que tem como objetivo fortalecer as iniciativas de transparência da Anvisa, levando conteúdo e conhecimento atualizado ao público. A transmissão é via web e a interação com os usuários é feita em tempo real, por um chat realizado durante o evento.
Confira a página específica de webinares realizados pela Agência.
Sistema Nacional de Controle de Receituários avança para controle de receitas especiais
Nova fase permitirá o controle eletrônico de receitas para medicamentos entorpecentes e psicotrópicos.
A Anvisa anuncia que está próxima de concluir uma importante evolução no Sistema Nacional de Controle de Receituários (SNCR). A evolução permitirá a emissão eletrônica de notificações de receitas amarelas e azuis, atualmente disponíveis apenas em formato físico.
Nas próximas semanas, o SNCR entrará em fase de testes com a nova funcionalidade, que permitirá a regulamentação do controle eletrônico das notificações de receita. Esses documentos, conhecidos como receituários amarelos e azuis, são utilizados para a prescrição de medicamentos entorpecentes e psicotrópicos, substâncias sujeitas a rigoroso controle devido ao seu potencial de uso indevido e dependência.
A regulamentação do controle eletrônico de notificações de receita representará um marco na modernização do controle de medicamentos sujeitos a controle especial, garantindo mais segurança, melhor rastreabilidade e mais eficiência no processo de prescrição e dispensação.
Acompanhe a evolução das etapas do projeto abaixo:
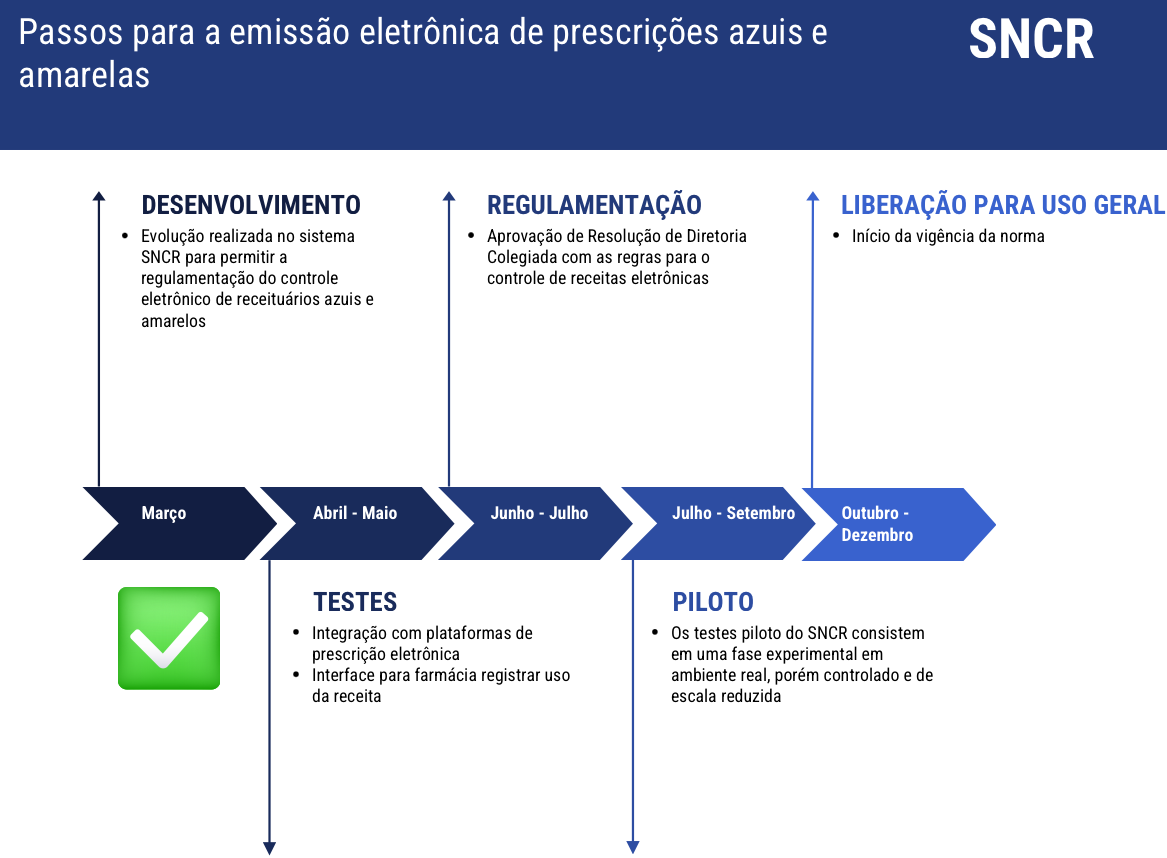
Gráfico - desenvolvimento da emissão eletrônica de prescrições azuis e amarelas
Padronização e Segurança
A implantação do Sistema Nacional de Controle de Receituários (SNCR), em vigor desde 18 de julho do ano passado, conforme a Resolução da Diretoria Colegiada (RDC) 873/2024, é um elemento essencial para garantir a validade nacional dos receituários. O sistema fornece numeração única nacional para profissionais prescritores previamente cadastrados e está disponível para as Vigilâncias Sanitárias em todo o território brasileiro.
O que muda com a evolução do SNCR?
Com a implementação do SNCR, será possível:
• Rastrear a prescrição eletrônica: acompanhar o ciclo de vida da receita, desde a prescrição até a dispensação na farmácia.
• Reduzir o risco de fraudes: diminuir a possibilidade de falsificações e desvios de receitas de medicamentos controlados.
• Aprimorar a fiscalização: facilitar o trabalho da Anvisa e das Vigilâncias de estados e municípios na identificação de irregularidades.
• Modernizar o sistema: adequar o controle de medicamentos controlados às novas tecnologias e à realidade da prescrição eletrônica.
Este avanço representa um passo significativo na transformação digital do controle especial de medicamentos e substâncias, visando tornar esse sistema de controle mais eficiente e seguro, beneficiando pacientes, profissionais de saúde e autoridades sanitárias em todo o país.
Fonte: Anvisa, em 08.04.2025.


